Definition und Ursache einer Netzhautablösung
Die Netzhaut ist die lichtempfindliche Schicht unseres Auges, auf der die Umwelt abgebildet wird. Sie leitet die Bildinformationen über den Sehnerven an das Gehirn weiter. Die Netzhaut ist nur Bruchteile eines Millimeters dick. Sie ist nur am Sehnerv und im Bereich der Ora serrata mit dem Augapfel verwachsen und wird durch eine aktive Pumpwirkung des unter ihr liegenden retinalen Pigmentepithels an die Augapfelwand angesogen.
Zu einer Netzhautablösung (Amotio retinae) kann es aus verschiedenen Gründen kommen. Am häufigsten ist die rissbedingte Netzhautablösung (rhegmatogene Amotio). Hierbei entsteht -z.B. bei einer altersbedingten Glaskörperabhebung und -schrumpfung- durch Zug des Glaskörpers ein Loch in der Netzhaut. Durch dieses Loch kann Flüssigkeit aus dem Glaskörperraum hinter die Netzhaut gelangen und sie abheben.
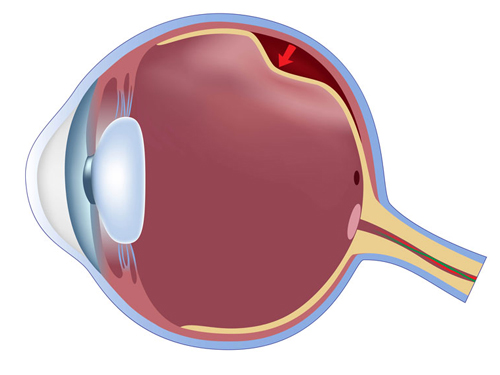
Ablösung der Netzhaut von der Aderhaut
Symptome einer Netzhautablösung
Einer Netzhautablösung können spezifische Symptome wie das Sehen von „Rußregen“, „Lichtblitzen“ oder eines „schwarzen Vorhangs“ vorausgehen.
Eine Netzhautablösung führt zu einem fortschreitenden Gesichtsfeldausfall und –unbehandelt- zur Erblindung des Auges.
Operation bei Netzhautablösung
Ziel aller Operationsverfahren ist es, die Netzhaut wieder anzulegen und Netzhautlöcher zu verschließen. Es werden zwei Prinzipien der Netzhautchirurgie unterschieden:
- Eindellende Operationen, bei denen der Augapfel von außen durch Aufnähen einer sog. „Plombe“ oder „Cerclage“ eingedellt wird, so dass die Netzhaut wieder ihren Untergrund berührt. Dieses seit Jahrzehnten bekannte Verfahren wird heutzutage vorzugsweise bei einfachen Ausgangssituationen angewandt.
- Eingriffe vom Augeninneren her, bei denen der Glaskörper entfernt wird (Vitrektomie) und die Netzhaut durch die Eingabe von gasförmigen oder flüssigen tamponierenden Substanzen wieder an ihre Unterlage angedrückt wird. Die tamponierenden Substanzen werden entweder vom Körper resorbiert (Gase) oder in einem weiteren Eingriff zu einem späteren Zeitpunkt wieder entfernt (Silikonöl).
Bei beiden Eingriffen müssen Netzhautlöcher durch eine ergänzende Laser- oder Kryobehandlung (Kältesonde) mit der darunter liegenden Schicht „verschweißt“ werden. Eingriffe zur Behandlung einer Netzhautablösung können zeitaufwendig sein. Sie werden daher in der Regel unter Allgemeinanästhesie vorgenommen.
In welchem Umfang die Sehfähigkeit wiederhergestellt werden kann, hängt vom Schweregrad der Erkrankung ab. Eine große Ausdehnung oder lange Dauer der Ablösung, das Vorhandensein von mehreren / großen Rissen oder eine Netzhautschrumpfung können nachteilige Faktoren sein. Eine frische, unkomplizierte Netzhautablösung kann in fast allen Fällen erfolgreich behandelt werden.

